
A lizoszómák az eukarióta sejtek fő lebontó és újrahasznosító központjai. Csoportunk elsősorban a népszerű Drosophila modellszervezetet használja a lizoszomális lebontási útvonalak genetikájának, sejtbiológiájának, biokémiájának, valamint élettani és patológiás szerepének és mechanizmusainak tanulmányozására. Az utóbbi időben érdeklődésünk kiterjedt arra is, hogy ezek az útvonalak koordinációja hogyan zajlik. Sejtbiológiai és biokémiai kísérleteinkkel tárjuk fel a lizoszómák dinamikus természetét emlős sejtkultúrákban és Drosophila szövetekben, valamint vizsgáljuk hogyan változik lipid- és fehérjeösszetételük éhezéskor, az agy öregedése során, illetve hogy miben különböznek egymástól az idegsejtek és a glia sejtek lizoszómái.
Legújabb projektjeink elsősorban három fő lizoszomális lebontási útvonalra koncentrálnak: az autofágiára, az endocitózisra és a fagocitózisra.
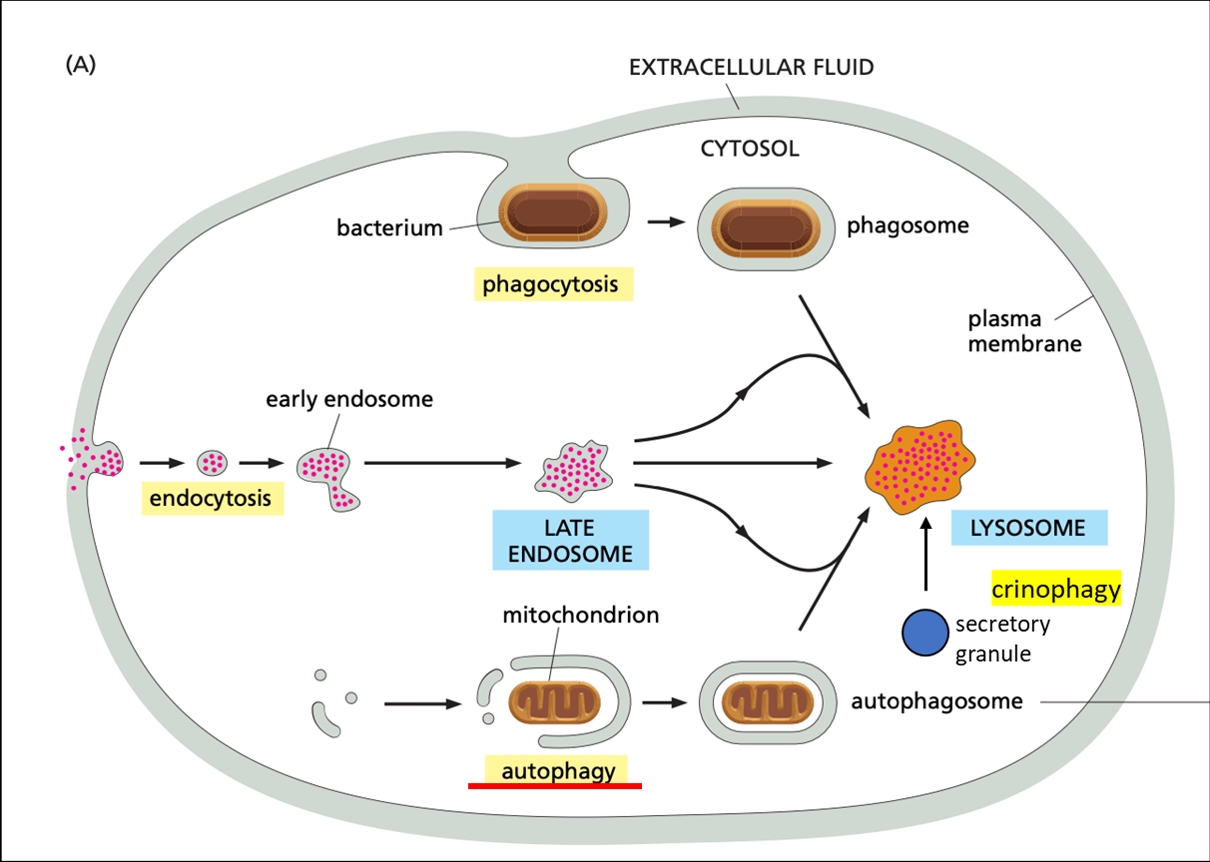
1. ábra. A lebontásra szánt anyagok fő szállítási útvonalai a lizoszómák felé. Az endocitózis felveszi az extracelluláris anyagokat, és endoszómákba csomagolja őket. A szállított anyagok általában makromolekulák és extracelluláris folyadék, továbbá a plazma membránban található receptorfehérjék. A fagocitózis egyfajta endocitózis, amely 0,5 μm-nél nagyobb részecskéket vesz fel sejtfelszíni receptorok segítségével. A lehetséges szállítmányok baktériumoktól és vírusoktól kezdve az azbeszthez hasonló inert anyagokon át a saját szervezetből származó partikulumokig, például az apoptotikus sejtekig terjednek. Az autofágia a sejten belüli komponenseket kettős membránú szállító vezikulumokba (autofagoszómákba) csomagolja, amelyek ezután lizoszómával egyesülnek. A szállítmány lehet sejtorganellum, makromolekulák és azok komplexei - többé-kevésbé véletlenszerűen kiválasztott citoplazmarészletekkel együtt. A krinofágia során a felesleges szekréciós granulumok lizoszómával történő közvetlen fúzió útján kerülnek lebontásra.
Autofágia
Az autofágia (a sejtek lizoszomális önemésztő tevékenysége) minden eukarióta sejtben zajlik. Az autofág aktivitás megnő például éhezéskor, és a felesleges sejtösszetevők újrahasznosításával biztosítja a túlélést. Az állatokban az autofágia az éhezés túlélésén túl további funkciókat is ellát, többek között szabályozza az élettartamot, a stresszreakciókat, a sejtek homeosztázisát, a sejthalált, az immunitást, a rákot, a neurodegeneratív betegségeket, az elhízást és a lipidanyagcserét. Az autofágia orvosbiológiai jelentősége mára már jól ismert, amit az is bizonyít, hogy a 2016-os Nobel díjat egy autofágiát élesztőben vizsgáló kutató kapta. A szelektív autofágia lehetővé teszi a specifikus sejtkomponensek (pl. sérült vagy felesleges sejtorganellumok, fehérjeaggregátumok és a sejteket megfertőző kórokozók) célzott felismerését, elkülönítését és eltávolítását speciális felismerő mechanizmusok segítségével. Jelenleg is vizsgáljuk az ubikvitinált fehérjék, az ER (endoplazmatikus retikulum) és a sérült lizoszómák szelektív lebontását (azaz az aggrefágiát, az ER-fágiát és a lizofágiát). Emellett az autofagoszómák és a lizoszómák közötti fúziós mechanizmusra, valamint annak lipidek és fehérjék általi szabályozására összpontosítunk. Ezen kísérletek során in vivo és in vitro módszerekkel azonosítjuk a fúziós mechanizmus bizonyos komponenseivel kölcsönható partnereket. A lehetséges biokémiai kötéseket in vitro rekonstruáljuk, majd biokémiai és genetikai elemzésekkel vizsgáljuk ezek funkcionális jelentőségét.
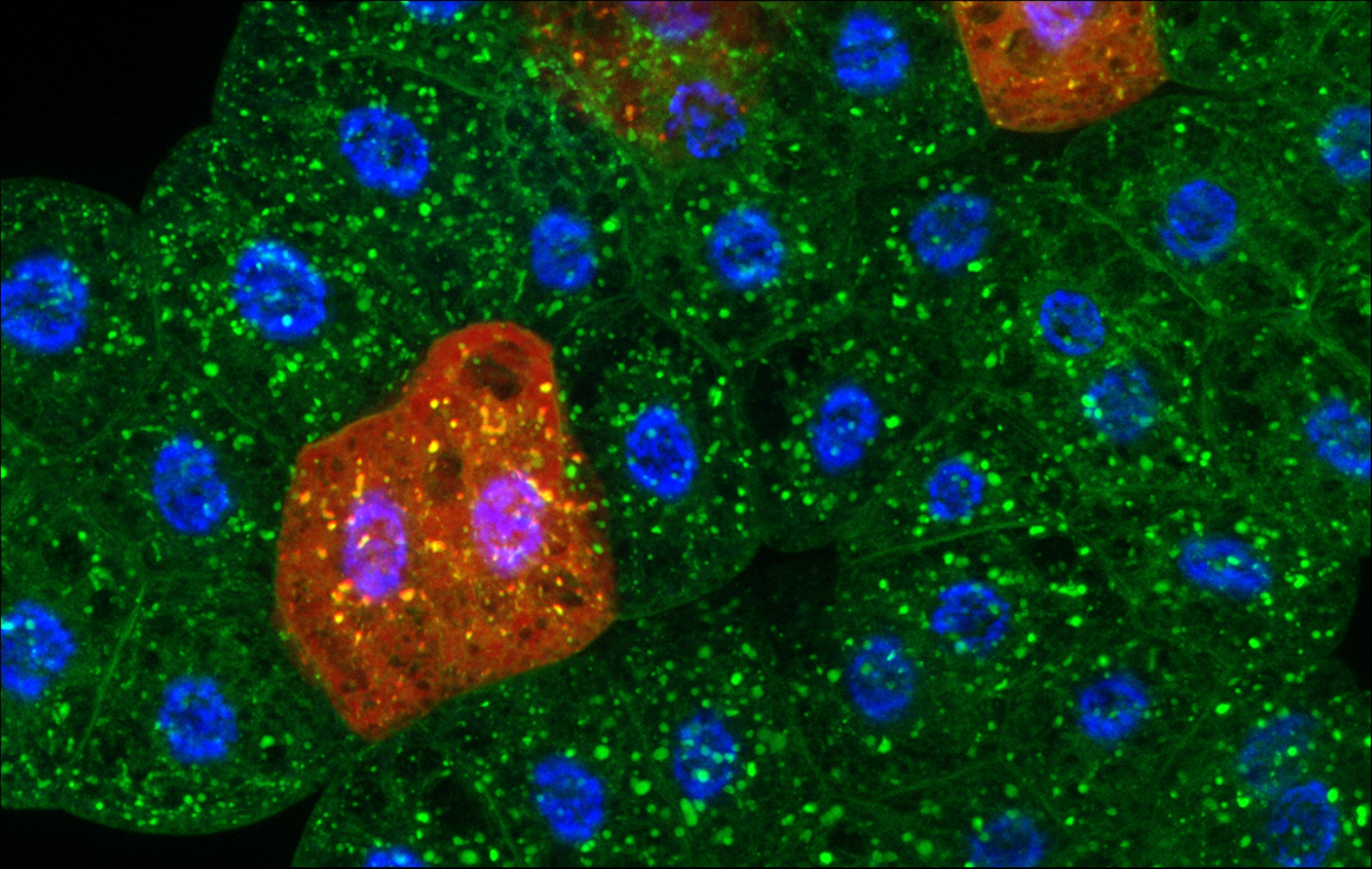
2. ábra. Éhezés által kiváltott ER-fágia genetikai mozaik módszerrel történő vizsgálata a Drosophila zsírszövetében. Ez a szerv funkcionálisan hasonló az emlősök májához és zsírszövetéhez, és éhezéses stresszre erős autofág indukcióval reagál. Ezért ebben a szövetben hatékonyan tanulmányozható az autofágia több formája, beleértve az ER-fágiát is, amely az endoplazmatikus retikulum (ER) szelektív lebontásáért felelős. A képen a Sec61-GFP (zöld) jelöli az ER-t, míg a piros színű sejtek azokat a mozaik sejtklónokat jelzik, amelyekben az egyik ER-fágia receptor gént csendesítettük.
Endocitózis
Az endocitózissal történő anyagfelvétel a normális sejtfunkció előfeltétele. Az endoszomális transzport hibái súlyos rendellenességekhez vezethetnek a sejtek és szervezetek működésében. Az eukarióta sejtek endoszomális hálózatában az endocitikus rakomány szállítása irányított mozgatást, érési folyamatot, és végül a transzport vezikulumok lizoszómákkal történő fúzióját foglalja magában. Az endoszomális éréshez több fehérje és multiprotein komplex közreműködése szükséges. Kutatásaink célja, hogy az ecetmuslica lárva magas endocitikus aktivitású nefrocitáit kísérleti modellként felhasználva megértsük a korábban még nem jellemzett, feltehető endocitikus funkcióval rendelkező fehérjék működését.
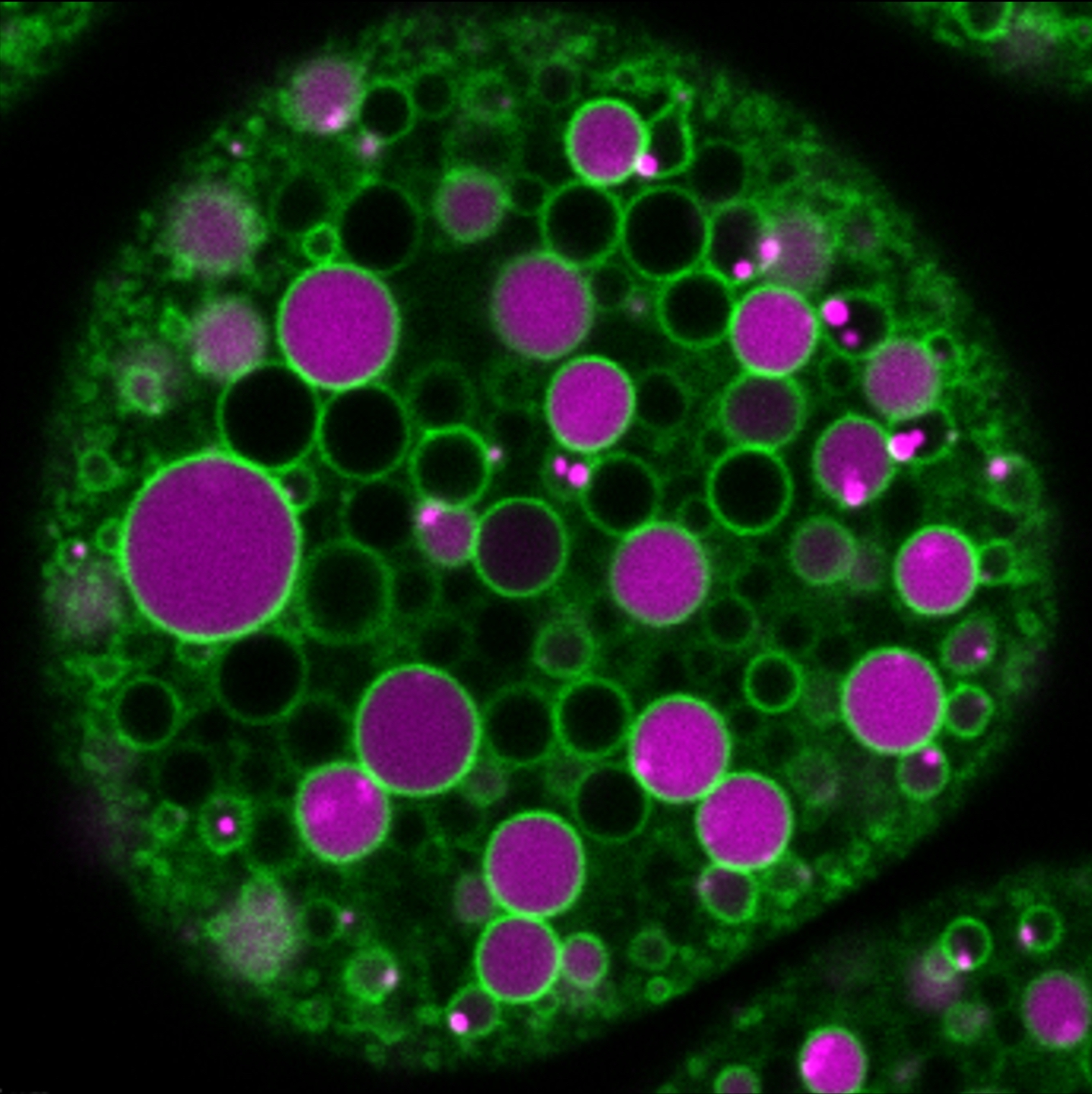
3. ábra: Konfokális mikroszkópos kép egy ex vivo tenyésztett élő nefrocitáról, amely fluoreszcens jelöléssel ellátott endocitikus nyomjelzőt (magenta) és fluoreszcens jelöléssel ellátott endoszómális fehérjét (zöld) tartalmaz. A nyomjelzőt a sejt endocitózis útján felveszi a tenyésztőközegből, majd gömb alakú endoszómákba szállítja. A zöld „gyűrűk” az endocitikus vezikulumokat jelölik, mivel egy fluoreszcensen jelölt fehérje a határoló membránba kerül. Az ilyen kísérleti felállások lehetővé teszik az endocitikus transzport vizsgálatát az endocitikus szállítmány és az endoszomális érési folyamat szabályozó fehérjéinek egyidejű megjelenítésével.
Fagocitózis
A fagocitózis során a sejten kívüli térből származó részecskék kerülnek bekebelezésre, amelyek normális esetben a lizoszómákba jutnak és lebomlanak. A professzionális fagocita sejtek, mint például a makrofágok, receptorokkal és adhéziós fehérjékkel vannak ellátva, citoszkeletonjuk pedig nagyon dinamikus, ami mind fontos fagocitikus képességük szempontjából. A fagocitózist két különböző sejttípusban tanulmányozzuk Drosophilában. Először is, makrofágokkal kapcsolatos kutatásaink az extracelluláris mátrix fragmentumok felvételének mechanizmusaira és fontosságára, valamint az apoptotikus törmelékek bekebelezésére (efferocitózis) összpontosítanak. Célunk az általános mechanisztikus résztvevők, valamint a fagocitózis adott altípusára jellemző tényezők azonosítása. Másodszor, a gliasejteket is tanulmányozzuk, amelyek normál körülmények között az idegrendszer egyedüli fagocitái. Nemrégiben fedeztük fel, hogy a gliák egy speciális, LC3-asszociált fagocitózis elnevezésű útvonalat használnak a sejtmaradványok eltávolítására sérülés után. Jelenleg azt vizsgáljuk, hogy ez a folyamat milyen szerepet játszik a légy látórendszerének megfelelő „behuzalozásában” a szinapszisok eltávolítása („pruning”) révén. Azt is tanulmányozzuk, hogy a gliasejtek hogyan hatnak az Alzheimer-kórhoz hasonló neurodegeneratív betegségek ellen, pl. a toxikus fehérjék fokozott lebontása révén.
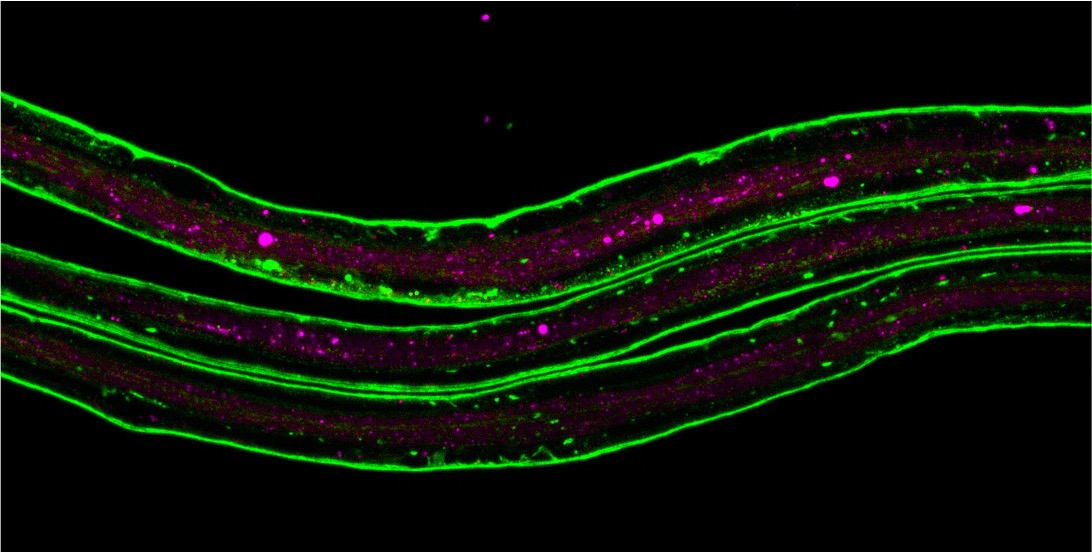
4. ábra. A képen a lárva abdominális idegei láthatók, ahol az egyik extracelluláris mátrix (ECM) fehérje, a laminin B1 zöld színnel, a gliasejtek lizoszómái pedig magenta színnel vannak jelölve. Ezt a rendszert használjuk annak feltárására, hogy a gliasejtek hogyan alakítják át ECM környezetüket a normális fejlődés során, illetve sérülés után a felesleges mátrix eltávolításával. A Drosophilában rendelkezésre álló hatékony genetikai eszközök segítségével szűrőrendszereket hoztunk létre a mátrix felvétel kulcsfontosságú tényezőinek azonosítására, amelyeket tovább vizsgálhatunk, hogy az ECM fragmensek fagocita által közvetített bekebelezésének mechanizmusát megértsük.
Selected papers
Selective autophagy fine-tunes Stat92E activity by degrading Su(var)2-10/PIAS in Drosophila glia. Vincze V, Esküdt Z, Fehér-Juhász E, Chhatre AS, Jipa A, Galambos AR, Feil-Börcsök D, Bence M, Juhász G, Szabó Á. Life Sci Alliance. 2026 Jan 7;9(3):e202503375. doi: 10.26508/lsa.202503375.
Lysosomal activity depends on TRPML1-mediated Ca2+ release coupled to incoming vesicle fusions. Bhattacharjee A, Abuammar H, Juhász G. J Biol Chem. 2024 Dec;300(12):107911. doi: 10.1016/j.jbc.2024.107911
PtdIns4P is required for the autophagosomal recruitment of STX17 (syntaxin 17) to promote lysosomal fusion. Laczkó-Dobos H, Bhattacharjee A, Maddali AK, Kincses A, Abuammar H, Sebők-Nagy K, Páli T, Dér A, Hegedűs T, Csordás G, Juhász G. Autophagy. 2024 Jul;20(7):1639-1650. doi: 10.1080/15548627.2024.2322493
LC3-associated phagocytosis promotes glial degradation of axon debris after injury in Drosophila models. Szabó Á, Vincze V, Chhatre AS, Jipa A, Bognár S, Varga KE, Banik P, Harmatos-Ürmösi A, Neukomm LJ, Juhász G. Nat Commun. 2023 May 29;14(1):3077. doi: 10.1038/s41467-023-38755-4.
Analysis of Drosophila Atg8 proteins reveals multiple lipidation-independent roles. Jipa A, Vedelek V, Merényi Z, Ürmösi A, Takáts S, Kovács AL, Horváth GV, Sinka R, Juhász G. Autophagy. 2021 Sep;17(9):2565-2575. doi: 10.1080/15548627.2020
Vps8 overexpression inhibits HOPS-dependent trafficking routes by outcompeting Vps41/Lt. Lőrincz P, Kenéz LA, Tóth S, Kiss V, Varga Á, Csizmadia T, Simon-Vecsei Z, Juhász G. Elife. 2019 Jun 13;8:e45631. doi: 10.7554/eLife.45631.
Molecular mechanisms of developmentally programmed crinophagy in Drosophila. Csizmadia T, Lőrincz P, Hegedűs K, Széplaki S, Lőw P, Juhász G. J Cell Biol. 2018 Jan 2;217(1):361-374. doi: 10.1083/jcb.201702145.
Microenvironmental autophagy promotes tumour growth. Katheder NS, Khezri R, O'Farrell F, Schultz SW, Jain A, Rahman MM, Schink KO, Theodossiou TA, Johansen T, Juhász G, Bilder D, Brech A, Stenmark H, Rusten TE. Nature. 2017 Jan 19;541(7637):417-420. doi: 10.1038/nature20815
Rab2 promotes autophagic and endocytic lysosomal degradation. Lőrincz P, Tóth S, Benkő P, Lakatos Z, Boda A, Glatz G, Zobel M, Bisi S, Hegedűs K, Takáts S, Scita G, Juhász G. J Cell Biol. 2017 Jul 3;216(7):1937-1947. doi: 10.1083/jcb.201611027.
Autophagosomal Syntaxin17-dependent lysosomal degradation maintains neuronal function in Drosophila. Takáts S, Nagy P, Varga Á, Pircs K, Kárpáti M, Varga K, Kovács AL, Hegedűs K, Juhász G. J Cell Biol. 2013 May 13;201(4):531-9. doi: 10.1083/jcb.201211160.

tudományos tanácsadó

tudományos főmunkatárs

tudományos főmunkatárs

tudományos munkatárs

tudományos munkatárs

tudományos munkatárs

tudományos munkatárs

tudományos munkatárs

tudományos munkatárs

tudományos munkatárs

tudományos segédmunkatárs

PhD hallgató

PhD hallgató

PhD hallgató

PhD hallgató

laboráns

ügyvivő szakértő

Szent-Györgyi hallgató
 JUHÁSZ Gábor
JUHÁSZ Gábor
|
tudományos tanácsadó | publikációk | CV |
 SZABÓ Áron
SZABÓ Áron
|
tudományos főmunkatárs | publikációk | CV |
 CSORDÁS Gábor
CSORDÁS Gábor
|
tudományos főmunkatárs | publikációk | CV |
 BLASTYÁK András
BLASTYÁK András
|
tudományos munkatárs | publikációk | CV |
 BÍRÓ Judit
BÍRÓ Judit
|
tudományos munkatárs | publikációk | CV |
 HARMATOS-ÜRMÖSI Adél
HARMATOS-ÜRMÖSI Adél
|
tudományos munkatárs | publikációk | CV |
 HEVÉRNÉ LACZKÓ-DOBOS Hajnalka
HEVÉRNÉ LACZKÓ-DOBOS Hajnalka
|
tudományos munkatárs | publikációk | CV |
 JIPA András
JIPA András
|
tudományos munkatárs | publikációk | CV |
 MARUZS Tamás
MARUZS Tamás
|
tudományos munkatárs | publikációk | CV |
 NAIK, Amruta
NAIK, Amruta
|
tudományos munkatárs | publikációk | CV |
 EVDOKIMOVA, Daniela
EVDOKIMOVA, Daniela
|
tudományos segédmunkatárs | publikációk | CV |
 CHHATRE, Aishwarya
CHHATRE, Aishwarya
|
PhD hallgató | publikációk | CV |
 VINCZE Virág
VINCZE Virág
|
PhD hallgató | publikációk | CV |
 PÉTER Lilla
PÉTER Lilla
|
PhD hallgató | publikációk | CV |
 DÉNES Dániel
DÉNES Dániel
|
PhD hallgató | publikációk | CV |
 BOZSÓ Szilvia
BOZSÓ Szilvia
|
laboráns | ||
 FEHÉRNÉ JUHÁSZ Erzsébet
FEHÉRNÉ JUHÁSZ Erzsébet
|
ügyvivő szakértő | publikációk | |
 ESKÜDT Zsombor
ESKÜDT Zsombor
|
Szent-Györgyi hallgató |