
Rövid bemutatkozás
A csoportunkban folytatott kutatások a fehérje - kismolekula kölcsönhatások, valamint fehérjék működési mechanizmusának megértésére irányulnak. A gyógyszerfejlesztési szempontból rendkívül jelentős G fehérje-kapcsolt receptorok in silico és in vitro kísérletes vizsgálatai útján szerkezet - hatás/funkció összefüggések megállapítására törekszünk. A csoport tevékenységei közé tartozik a vizsgálatokhoz szükséges, stabil ill. radioaktív izotópokkal, fluorofórokkal jelzett vagy nem természetes építőkövet tartalmazó kismolekulák, peptidek, fehérjék előállítása, valamint membrán-asszociált félszintetikus fehérjék előállítását célzó kémiai módszerek kidolgozása.
Folyamatban lévő kutatási projektek
1. G fehérje-kapcsolt receptorok működésének szerkezeti mechanizmusa (Borics A.)
A G fehérje-kapcsolt receptorok (GPCR-ek) a human genom egyik legnagyobb fehérjecsaládját alkotják és számos alapvető élettani funkcióban vesznek részt. Ennek következtében a GPCR-ek sok betegség kialakulásában is szerepet játszanak., melynek köszönhetően a kereskedelmi forgalomban lévő, vényköteles gyógyszerek hozzávetőlegesen egy harmadát e receptorcsalád tagjait célzó készítmények teszik ki. Számos GPCR atomi részletességű, aktív és inaktív állapotú szerkezete ismeretes de az aktív és inaktív állapotok közötti átalakulás szerkezeti mechanizmusa még nem teljesen ismert. Kutatásaink során ligandum-receptor kölcsönhatások szerepét vizsgáljuk a receptor elektrosztatikai egyensúlyára gyakorolt hatásuk tükrében, a receptorcsalád általános sajátságainak megismerését célozva. Vizsgálataink egy új szermlélet bevezetésén alapulnak, mely a receptor belsejében lévő töltéseloszlásra fektet hangsúlyt. Legfrissebb molekuladinamikai szimulációs viszgálataink során kimutattuk, hogy a m-opioid receptor esetében a külső stimulus a 7. transzmembrán helixen elhelyezkedő, fokozottan konzervált, poláris aminosav oldalláncok korreláló mozgásai útján továbbítódik a receptor intracelluláris felszíne irányába. E megfigyelés alapján feltételezzük, hogy a GPCR-ek aktivációjának kiindulási lépése az ortosztérikus ill. allosztérikus kötőhelyek és az intracelluláris G fehérje-kötő felület közötti töltésegyensúly-eltolódás. A kutatás további A osztályú GPCR-ekre, a b2-adrenerg és I-es típusú kannabinoid receptorokra való kiterjesztése során a fenti hipotézis további megerősítést nyert. Mind a három vizsgált receptor esetén azonosítottunk egy konzervált aminosavak ill. motívumok által alkotott poláris jelátviteli csatornát, mely a receptorok ligandumkötő zsebe és az intracelluláris G fehérje-kötő felszíne között húzódik. A m-opioid receptor esetében mutációs és in vitro farmakológiai kísérletekkel kimutattuk, hogy a csatornát alkotó aminosavak módosításai a receptor ligandumkötő és aktivációs képességének megszűnéséhez vezetnek. Jelenleg a receptorok aktivációjáért felelős specifikus receptor-ligandum kölcsönhatásokat vizsgáljuk de novo kölcsönhatás-specifikus ligandumok, mutáns receptorok, in vitro funkcionális vizsgálatok, kevert kvantum- és klasszikus mechanikai számítások (QM/MM) és szaturáció-transzfer tripla differencia (STTD) 1H-NMR spektroszkópiás módszerek alkalmazásával.
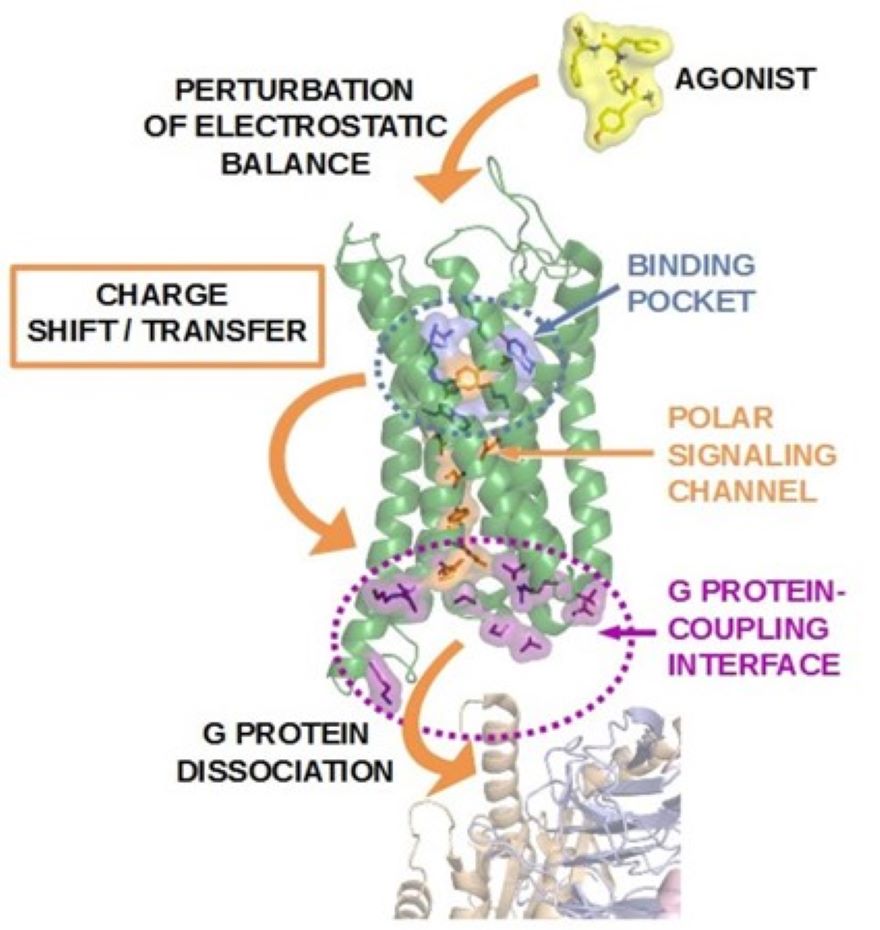
1. Ábra: G fehérje-kapcsolt receptorok feltételezett aktivációs mechanizmusa
2. Az I-es típusú kannabinoid receptorokon allosztérikusan ható, szintetikus kannabinoidok toxicitását csökkentő hatóanyagok fejlesztése (Dvorácskó Sz.)
Az endokannabinoid rendszer számos élettani funkció és kóros folyamat szabályozásában vesz részt a központi idegrendszerben és a perifériás szervekben egyaránt. A kannabinoid receptorokkal (CBR) kölcsönhatásba lépő vagy az endokannabinoid jelátvitelt moduláló szintetikus vegyületek gyógyászati potenciállal rendelkeznek neurológiai betegségek, pszichiátriai rendellenességek, neuropátiás fájdalom és elhízás kezelésében. Számos jótékony hatásuk ellenére a növényi eredetű és a szintetikus CBR-ligandumok klinikai alkalmazását a pszichoaktív hatásuk korlátozza. Továbbá a tiltott szerek között világszerte rendkívül erős szintetikus CB1R agonisták is találhatók, amelyek toxikus, akár halált okozó vegyületek és gyakran ismeretlen klinikai hatásokkal, változatos farmakodinámiával és farmakokinetikával rendelkeznek. Jelenleg nincs specifikus antidotum az ilyen szintetikus kannabinoid mérgezések kezelésére. Nemrégiben írtak le egy egyedülálló endogén peptidcsaládot (hemopresszinek vagy pepcanok), amelyek szerkezetileg különböznek az endogén lipid kannabinoidoktól, de kölcsönhatnak a CBR-kal. Közülük a pepcan-12 a legnagyobb mennyiségben előforduló peptid, amelyről kimutattuk, hogy pszichoaktív mellékhatás nélkül képes a rágcsálókban szorongást, táplálékfelvételt, bélmotilitást és fájdalomcsillapítást modulálni. A saját és más csoportok in vitro eredményei szerint a pepcan-12 a CB1R negatív allosztérikus modulátora, ezért feltételezzük, hogy a pepcan-12 és szintetikus analógjai kiváló vezérvegyületek pszichoaktív mellékhatások nélküli, CBR-kon ható peptid hatóanyagok kifejlesztésére. Ezen projekt keretében a módosított pepcan peptidek előállítását, majd részletes farmakológiai és molekuláris jellemzését követően magatartási szinten vizsgáljuk meg hatásukat.
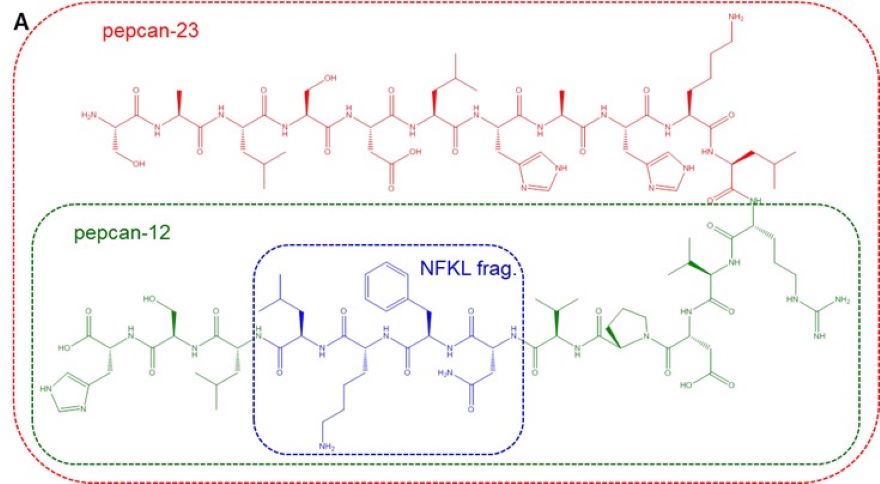

2. Ábra: Pepcanok és hemopresszinek módosító hatásai: (A) szerkezet (B) kölcsönhatás az I-es típusú kannabinoid receptorral (C) funkcionális aktivitás
Félszintetikus lipoproteinek exogén módon történő plazma membránba juttatása lehetővé teszi a sejtmembrán tervezett és kontrollált módosítását. Így ez a stratégia alkalmas membránfehérjék dinamikai vizsgálatára, membránfehérjék sejten belüli körforgásának tanulmányozására, valamint biológiailag aktív fehérjék és terápiás sejtek hatásosságának növelésére. Erre a célra egy olyan módszert dolgoztunk ki, amely lehetővé teszi, hogy élő sejtekkel kompatibilis körülmények között építsünk funkcionális fehérjéket a sejtmembrán felszínére. Bemutattuk, hogy amfifil koleszterin származékokkal kapcsolt fehérjék élő sejtek membránjának külső rétegébe horgonyozhatók. Az optimalizált koleszterin származékok vízoldékonyak, nem toxikusak és detergensek nélkül alkalmazhatók sejtkultúrákban. Mivel a horgony molekulák fejcsoportja fluoreszcens vagy radioaktív jelet tartalmaz, így lehetővé teszik a kapcsolt fehérje direkt képalkotásos leképezését. Továbbá a koleszterin képes a szfingolipidek környezetében dúsulni, ezért a koleszterin alapú horgony molekulák alkalmasak a kapcsolt fehérjék lipid raftokba történő bejuttatására is. A horgony molekuláink mindezen tulajdonságainak bemutatására az mCherry fluoreszcens fehérje, valamint a teljes hosszúságú prion fehérje C-terminmális végéhez kapcsoltunk koleszterin horgonyt, majd a kapott lipoproteineket SHSY-5Y neuroblasztóma sejtek membránjába horgonyoztuk. A koleszterin horgonyok membránbeli elhelyezkedésének atomi részleteit elméleti módszerek segítségével írtuk le.
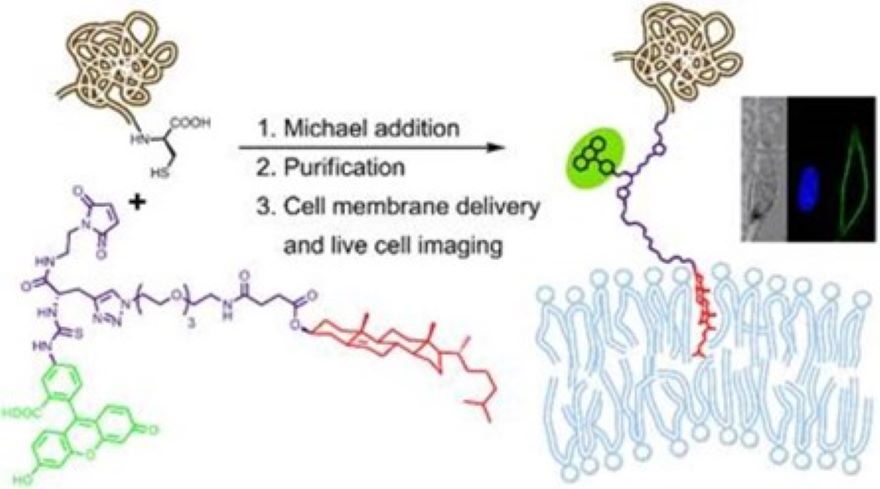
3. Ábra. Szintetikus módszer félszintetitkus fehérjék szimultán fluoreszcens jelölésére és membránba horgonyzására.
4. mRNS vakcina lipidek (Tömböly Cs.)
Nukleozid-módosított hírvivő RNS (mRNS) lipid nanorészecske formulációk (LNP) segítségével a sejtek transzfektálásán keresztül vakcinálási és más immunterápiás célok megvalósíthatók. Az LNP-k egyik kulcsfontosságú összetevői az ionizálható lipidek, amelyek zsírsavlánchoz kapcsolódó ionizálható fejcsoportból álló amfifil molekulák. A Biotechnológiai Nemzeti Laboratóriummal együttműködve célunk egy saját, moduláris ionizálható lipidkönyvtár létrehozása, többek között az afrikai sertéspestis vírus (ASFV) elleni vakcina létrehozásához és optimalizálásához. A modularitás ezen túl lehetővé teszi olyan lipidek szintézisét, amellyel az mRNS-LNP formulációk farmakológiai tulajdonságai finomhangolhatók az adott célnak megfelelően.
Válogatott közlemények
Sarkar A, Mitra A, Borics A. All-Atom Molecular Dynamics Simulations Indicated the Involvement of a Conserved Polar Signaling Channel in the Activation Mechanism of the Type I Cannabinoid Receptor. Int J Mol Sci. 2023, 24, 4232. doi: 10.3390/ijms24044232.
Dvorácskó Sz, Herrerias A, Oliverio A, Bhattacharjee P, Pommerolle L, Liu Z, Feng D, Lee Y-S, Hassan SA, Godlewski G, Cinar R, Iyer MR. Cannabinoformins: Designing biguanide-embedded, orally available, peripherally selective cannabinoid-1 receptor antagonists for metabolic syndrome disorders, J. Med. Chem., 2023, 66, 11985-004. doi:10.1021/acs.jmedchem.3c00599.
Dvorácskó Sz, Dimmito MP, Sebastiani J, La Regina G, Silvestri R, Pieretti S, Stefanucci A, Tömböly Cs, Mollica A. Rimonabant-Based Compounds Bearing Hydrophobic Amino Acid Derivatives as Cannabinoid Receptor Subtype 1 Ligands. ACS Med Chem Lett, 2023, 9, 479-486. doi: 10.1021/acsmedchemlett.3c00024
Mitra A, Sarkar A, Borics A. Universal Properties and Specificities of the β2-Adrenergic Receptor-Gs Protein Complex Activation Mechanism Revealed by All-Atom Molecular Dynamics Simulations. Int J Mol Sci. 2021, 22, 10423. doi: 10.3390/ijms221910423.
Mitra A, Sarkar A, Szabó MR, Borics A. Correlated Motions of Conserved Polar Motifs Lay out a Plausible Mechanism of G Protein-Coupled Receptor Activation. Biomolecules. 2021, 11, 670. doi: 10.3390/biom11050670.
Dvorácskó Sz, Keresztes A, Mollica A, Stefanucci A, Macedonio G, Pieretti S, Zádor F, Walter F, Deli M, Kékesi G, Bánki L, Tuboly G, Horváth Gy, Tömböly Cs. Preparation of bivalent agonists for targeting the mu opioid and cannabinoid receptors. Eur. J. Med. Chem. 2019, 178, 571-88. doi: 10.1016/j.ejmech.2019.05.037
Váradi A, Marrone GF, Palmer TC, Narayan A, Szabó MR, Le Rouzic V, Grinnell SG, Subrath JJ, Warner E, Kalra S, Hunkele A, Pagirsky J, Eans SO, Medina JM, Xu J, Pan YX, Borics A, Pasternak GW, McLaughlin JP, Majumdar S. Mitragynine/Corynantheidine Pseudoindoxyls As Opioid Analgesics with Mu Agonism and Delta Antagonism, Which Do Not Recruit β-Arrestin-2. J Med Chem. 2016, 59, 8381-97. doi: 10.1021/acs.jmedchem.6b00748.
Schäfer B, Orbán E, Borics A, Huszár K, Nyeste A, Welker E, Tömböly C. Preparation of semisynthetic lipoproteins with fluorescent cholesterol anchor and their introduction to the cell membrane with minimal disruption of the membrane. Bioconjug Chem. 2013, 24, 1684-97. doi: 10.1021/bc4002135.
Tóth G, Borics A. Closing of the flaps of HIV-1 protease induced by substrate binding: a model of a flap closing mechanism in retroviral aspartic proteases. Biochemistry. 2006, 45, 6606-14. doi: 10.1021/bi060188k.
Szabadalmak
Iyer MR, Dvorácskó Sz, Bhattacharjee P, Cinar R, Kunos G. PCT Patent Application No. PCT/U2023/014846 Cannabinoid receptor modulating compounds)
Mollica A, Macedonio G, Stefanucci A, Dvorácskó Sz, Tömböly Cs. Indazole derivatives as modulators of the cannabinoid system. EP18170728 (elbírásás alatt)
Alkalmazott technikák
Kémiai laboratóriumi módszerek
Szilárd- és oldatfázisú peptidszintézis (pl. hemopresszinek, opioid peptidek)
Kis szerves molekulák tervezése és szintézise (pl. szintetikus kannabinoidok)
Bioaktív vegyületek radioaktív jelölése
Preparatív és analitikai elválasztási technikák
Proteolitikus degradáció vizsgálat
Illegális szintetikus kannabinoidiok bűnügyi laboratóriumi vizsgálata
Számításos kémiai módszerek
Molekuladinamika (konvencionális, replica exchange, szimulált anelláció, irányított, folding, stb.)
Molekuláris dokkolás (fehérje-kismolekula, fehérje-fehérje)
Kis szerves molekulák és nemtermészetes aminosavak molekulamechanikai parametrizálása
Fehérjék térszerkezet-predikciója
Kvantumkémiai számítások
Rezgési spektrumok számítása
In vitro farmakológiai technikák
Állati szövetpreparátumok készítése, sejtkultúrákkal végzett munka
Radioligandum-receptor kötődési mérések
Radioligandum [35S]GTPγS funkcionális mérés
TR-FRET funkcionális mérés (cAMP)
Kemilumineszcens funkcionális mérés (β-arrestin-2 kötődés)
ELISA (AMPK aktivitás) mérés
Radioligandum NOS aktivitás mérés
In vivo farmakológiai technikák
Gyógyszeradagolási és kezelési kísérletek
Farmakokinetikai és szöveteloszlási vizsgálatok
Funkcionális mérések
Viselkedési kísérletek (elevated plus maze assay, alcohol drinking models)
’Tetrad test’ (locomotion, body temperature, hot plate analgesia, catalepsy)

tudományos főmunkatárs

tudományos munkatárs

PhD hallgató

tudományos segédmunkatárs

laboráns

tudományos főmunkatárs (jelenleg külföldön)
 BORICS Attila
BORICS Attila
|
tudományos főmunkatárs | publikációk | CV |
 DVORÁCSKÓ Szabolcs
DVORÁCSKÓ Szabolcs
|
tudományos munkatárs | publikációk | CV |
 SARKAR Arijit
SARKAR Arijit
|
PhD hallgató | publikációk | CV |
 KÖDMÖN Ádám
KÖDMÖN Ádám
|
tudományos segédmunkatárs | CV | |
 TÓTHNÉ PAPP Éva
TÓTHNÉ PAPP Éva
|
laboráns | ||
 TÖMBÖLY Csaba
TÖMBÖLY Csaba
|
tudományos főmunkatárs (jelenleg külföldön) | publikációk | CV |